Wissenschaftlicher Artikel von:
Dr. med. Maximilian Witzel ist Studienarzt der Wiskott-Aldrich Gentherapie Studie am Dr. von Haunerschen Kinderspital der Ludwigs-Maximilians-Universität in München. Neben der Durchführung der klinischen und Labor-chemischen Nachsorge-Untersuchungen, arbeitet er in der Arbeitsgruppe von Prof. Dr. Klein an der Aufklärung bisher unbekannter Immundefekte im Kindesalter.
Prof. Dr. Christoph Klein ist Direktor des Dr. von Haunerschen Kinderspitals der Ludwigs-Maximilians-Universität in München. Christoph Klein widmet sein wissenschaftliches Interesse der Schnittstelle zwischen klinischer Medizin und Immunologie, insbesondere dem Verständnis über die menschlichen Erkrankungen des Blutes und des Immunsystems.
Hier können Sie den Artikel als PDF Datei herunterladen.

Worum geht es?
Das Wiskott-Aldrich Syndrom ist eine seltene Erkrankung des Immunsystems. Nach europäischer Definition ist eine Erkrankung selten, wenn weniger als fünf von 10.000 Menschen von ihr betroffen sind. Jede einzelne Erkrankung ist somit zwar selten, doch in ihrer Gesamtheit betreffen die seltenen Erkrankungen allein in Europa rund 30 Millionen Menschen. Seltene Erkrankungen haben häufig einen genetischen, oft monokausalen Ursprung. Ein wichtiges Ziel ist es, die genetische Ursache seltener Erkrankungen zu identifizieren, um rasch eine korrekte Diagnose stellen zu können. Der Beitrag der Forschung ist hier von geradezu unmessbarer Bedeutung. In Deutschland haben sich daher Forschungsverbünde zusammengeschlossen, um die deutschlandweit bestehende Expertise zu ausgewählten Gruppen seltener Erkrankungen zu bündeln. Die Verbünde engagieren sich in der Grundlagen-, Therapie- und Versorgungsforschung.
Einer dieser Verbünde ist PID-Net, das deutsche Netzwerk für primäre Immundefekt-erkrankungen. In diesem Verbund wird unter anderem eine Gentherapie für Wiskott-Aldrich Syndrom weiter erforscht. Das übergeordnete Ziel dieses Projektes ist es, langfristig die Effizienz und Sicherheit einer klinischen hämatopoetischen Stammzell-Gentherapiestudie für Patienten mit Wiskott-Aldrich-Syndrom zu untersuchen und innovative Gentherapie-strategien für Patienten mit monogenetischen Defekte des Immunsystems weiterzuentwickeln. Das große Potential einer hämatopoetischen Stammzell-Gentherapie liegt darin, dass die Stammzellen des betroffenen Patienten korrigiert werden können. Hierdurch kann eine Knochenmarktransplantation von einem fremden Spender umgangen werden. Eine Knochenmarktransplantation kann mit einer hohen Morbidität und Mortalität assoziiert sein – abhängig vom klinischen Zustand des Patienten, der zugrundeliegenden Erkrankung und der Übereinstimmung von HLA-Merkmalen zwischen Spender und Empfänger.
Die hämatopoetische Stammzell-Gentherapie zur Behandlung des Wiskott-Aldrich Syndroms
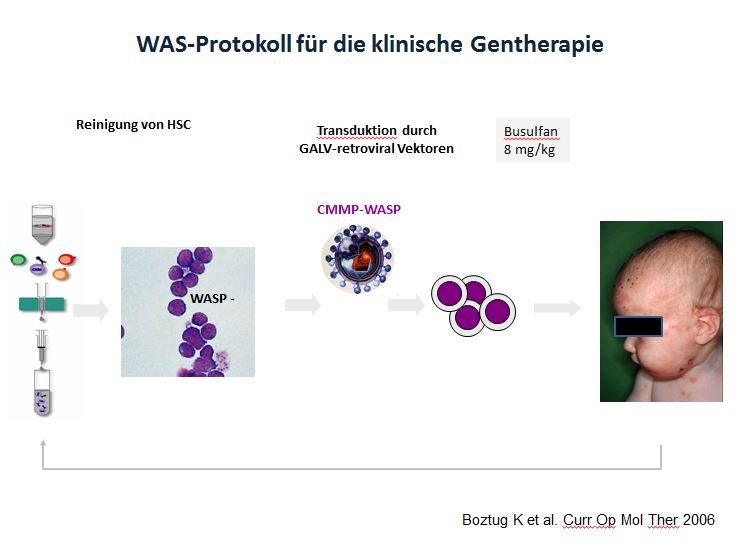
Das Wiskott-Aldrich Syndrom (WAS) ist eine x-chromosomale Erkrankung, die durch hemizygote Mutation im Wiskott-Aldrich Gen (WAS) verursacht werden kann. Der Phänotyp umfasst Thrombozytopenie, Immundefizienz, Autoimmunität und eine Prädisposition zu Malignomen. Das bedeutet, dass sich Betroffene durch eine hohe Anfälligkeit für lebensbedrohliche Infektionen, Ekzeme sowie eine starke Blutungsneigung auszeichnen. Patienten mit klassischem WAS versterben meist in den ersten beiden Lebensdekaden. Bisher bestand die einzige kurative Therapie in einer allogenen Knochenmark-transplantation. Eine allogene Knochenmarktransplantation ist mit einem erheblichen Morbiditäts- und Mortalitätsrisiko assoziiert, insbesondere, wenn ein HLA-identischer Spender nicht verfügbar ist. WASp wird ausschließlich in hämatopoetische Zellen exprimiert, so dass die autologe Transplantation von korrigierten hämatopoetischen Stammzellen (HSC) eine innovative therapeutische Option darstellt. 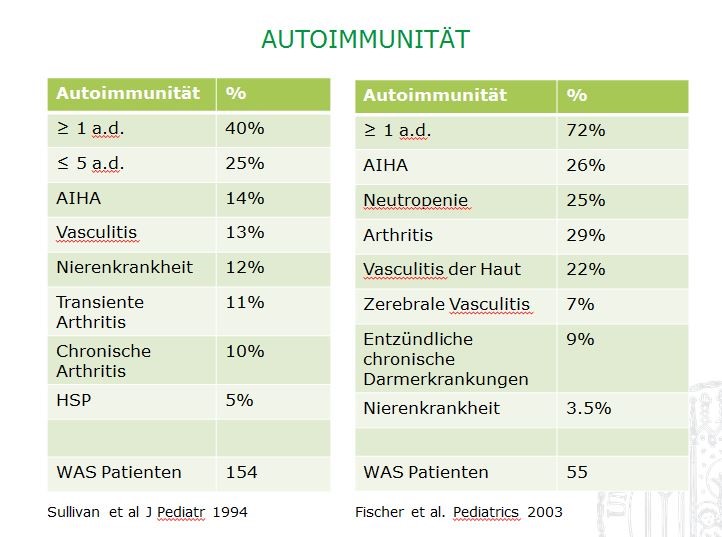
- Abb.1: Neben der klassischen Trias aus Thrombozytopenie, Infektneigung und Ekzemen, neigen Wiskott-Aldrich Syndrom Patienten in hohem Maße zu Autoimmunerkrankungen. (a.d.:Autoimmunmanifestation) adaptiert nach Sullivan et al. 1 und Fischer et al. 2.
Prinzipien der hämatopoetischen Stammzell Gentherapie (HSC GT):
Bei der HSC GT wird in die autologe Stammzellen eines betroffenen Patienten mit Hilfe eines viralen Vektors ein therapeutisches Gen (Transgen) eingeschleust. Die korrigierten HSC werden nach verschiedenen Sicherheitskontrollen dem Patienten zurückgegeben. Im Idealfall kommt es mit einer Latenz von mehreren Monaten zum Engraftment (Anwachsen) der therapeutisch modifizierten HSC, die daraus resultierenden Zelllinien tragen eine Kopie des Transgens und sind funktionell korrigiert. HSC GT Studien zur Behandlung des X-chromosomalen schweren kombinierten Immundefekts (X-SCID) 3, 4, der Adenosin Deaminase Mangel (ADA-SCID)5, und der Chronischen Granulomatose (CGD)6, haben klinischen Erfolge und zeitweise die funktionelle Korrektur von Immunzellen gezeigt. Allerdings sind hierbei schwerwiegende Nebenwirkungen aufgetreten (Insertionsmutagenese, Vektor-Inaktivierung).

- Abb.2: Prinzipien der hämatopoetischen Stammzell-Gentherapie: Zunächst wird das therapeutische Transgen in einen Vektor kloniert (hier: Vektor mit WASP). Mit Hilfe von Verpackungsplasmiden werden virale Partikel hergestellt (Packaging Cells, Viral Production). Nach Entnahme der hämatopoetischen Stammzellen des Patienten werden diese mit Hilfe der viralen Partikel korrigiert. Die viralen Partikel dienen als Genfähre für das therapeutische Gen.
Erste HSC zur Behandlung des Wiskott-Aldrich Syndroms:
Bis heute haben zehn Kinder mit Wiskott-Aldrich-Syndrom im Rahmen einer klinischen Studie die neue Behandlung erhalten. In der von uns durchgeführten Gentherapiestudie7 zur Behandlung von WAS konnte in 9/10 Patienten eine Engraftment der korrigierten Stammzellen (HSC) festgestellt werden. Patienten mit klassischem WAS exprimieren meist kein Wiskott-Aldrich Syndrom Protein (WASp). Nach HSC GT konnte die de novo Expression von WASp in den Zellen der lymphozytären und myeloide Reihe sowie den Thrombozyten nachgewiesen werden. Funktionell konnte eine teilweise oder eine vollständige Rekonstitution des Immundefekts, der Autoimmunität und der Blutungsneigung dokumentiert werden. Insbesondere zeigte sich nach HSC GT die Korrektur der T Zell Funktion (Wiederherstellung eines polyklonalen T-Zell Rezeptor Repertoires), der B-Zellfunktion (die Generation einer suffizienten Impfantwort nach Impfung) sowie die Korrektur der NK Zellfunktion (Ausbildung von NK-Zellsynapsen mit spezifischer NK Zell Lyse Kapazität). Einhergehend mit einem Anstieg der Thrombozytenzahlen und Thrombozytenvolumina zeigten alle Patienten eine deutliche Verringerung der Blutungsneigung 8.
Die Analyse der Insertionstellen im Genom der Patienten zeigte zunächst eine polyklonale Hämatopoese. Im Verlauf zeigte sich jedoch bei 7 Patienten eine akute Leukämie (1 Akute Myeloide Leukämie (AML), 4 Akute T Zell Lymphoblastische Leukämien (T-ALL), 2 primäre T-ALL mit tertiärer AML). Zum Zeitpunkt der Leukämiediagnostik zeigte sich ein Anstieg des klonalen Beitrags von Insertionstellen in der Nähe von LMO2 (T-ALL), MDS1 (AML) oder MN1 (AML). Die genetischen Analysen der Leukämiezellen zeigten weitere zytogenetische Veränderungen wie zB. chromosomale Translokationen8 . LMO2 ist ein bekanntes Onkogen, was bei der Entstehung von 10-20% der T-ALL 9 unabhängig von einer HSC GT eine wichtige Rolle spielt. Auch im Rahmen der HSC GT zur Behandlung des X1 SCID wurde eine Aktivierung von LMO2 im Rahmen der Leukämieentstehung beobachtet4, Insertionen in der Nähe des MDS1 Onkogenlokus waren mit der Entstehung Myelodysplasticher Syndrome nach HSC GT zur Therapie der CGD 6 assoziiert.
Die aufgetretenen schwerwiegenden Nebenwirkungen zeigen die aktuellen Grenzen der γ retroviralen hämatopoetischen Stammzell-Gentherapie auf. Die Verwendung von SIN-lentiviralen Vektoren für die WAS Gentherapie, wie sie zurzeit u.a. in Mailand, Paris, Boston und London (siehe auch 10 für aktive HSC GT) durchgeführt wird, kann möglicherweise das Risiko der Leukämientstehung reduzieren. 11 Langzeitbeobachtungen stehen derzeit noch aus.
Durch ihren autologen Ansatz, d.h. die Verwendung Patienten-eigener Stammzellen, ist die HSC GT zur Behandlung monogenetischer Krankheiten eine innovative Behandlungsmethode mit hohem Zukunftspotential. Patienten mit einer schwerwiegenden Erkrankung des Immunsystems kann bisher oft nur durch eine Knochenmarktransplantation geholfen werden. Für viele dieser Patienten ist kein HLA-identischer Spender verfügbar. In dieser Situation kann eine hämatopoetische Stammzell- Gentherapie eine wichtige therapeutische Alternative darstellen. Im Rahmen des PID-Net Konsortium besteht das Ziel, eine erfolgreiche, nachhaltige und sichere Gentherapie für viele primäre Immundefekterkrankungen zu entwickeln.
Informationen zu den Autoren:
Dr. med. Maximilian Witzel ist Studienarzt der Wiskott-Aldrich Gentherapie Studie am Dr. von Haunerschen Kinderspital der Ludwigs-Maximilians-Universität in München. Neben der Durchführung der klinischen und Labor-chemischen Nachsorge-Untersuchungen, arbeitet er in der Arbeitsgruppe von Prof. Dr. Klein an der Aufklärung bisher unbekannter Immundefekte im Kindesalter.
Prof. Dr. Christoph Klein ist Direktor des Dr. von Haunerschen Kinderspitals der Ludwigs-Maximilians-Universität in München. Christoph Klein widmet sein wissenschaftliches Interesse der Schnittstelle zwischen klinischer Medizin und Immunologie, insbesondere dem Verständnis über die menschlichen Erkrankungen des Blutes und des Immunsystems. Ein bahnbrechender Erfolg seiner Arbeitsgruppe war die Auflösung eins über 50 Jahre dauernden Rätsels. Durch die Identifizierung von Mutationen im Gen HAX1 war es möglich, die Ursache des Morbus Kostmann, historisch gesehen der ersten beschriebenen primären Immundefekterkrankung, aufzuklären. Sein Team hat weltweit erstmalig Patienten mit einem seltenen Immundefektsyndrom, dem Wiskott-Aldrich-Syndrom, mittels Gentherapie behandelt. Christoph Klein ist Sprecher des Sprecherrates der deutschen Forschungsverbünde für seltene Erkrankungen, Leiter des deutschen Forschungsverbundes PID-NET: Netzwerk für primäre Immundefekterkrankungen und hat außerdem eine Stiftung für Kinder mit seltenen Erkrankungen ins Leben gerufen (Care-for-Rare). Die Care-for-Rare Allianz bietet eine einzigartige Plattform, Kindern mit seltenen Erkrankungen weltweit Zugang zu modernen diagnostischen und therapeutischen Verfahren zu schaffen.
Quellen:
1. Sullivan KE, Mullen CA, Blaese RM, Winkelstein JA. A multiinstitutional survey of the Wiskott-Aldrich syndrome. The Journal of pediatrics 1994 Dec;125(6 Pt 1):876-85.
2. Dupuis-Girod S, Medioni J, Haddad E, Quartier P, Cavazzana-Calvo M, Le Deist F, et al. Autoimmunity in Wiskott-Aldrich syndrome: risk factors, clinical features, and outcome in a single-center cohort of 55 patients. Pediatrics 2003 May;111(5 Pt 1):e622-7.
3. Gaspar HB, Cooray S, Gilmour KC, Parsley KL, Adams S, Howe SJ, et al. Long-term persistence of a polyclonal T cell repertoire after gene therapy for X-linked severe combined immunodeficiency. Science translational medicine 2011 Aug 24;3(97):97ra79.
4. Hacein-Bey-Abina S, Garrigue A, Wang GP, Soulier J, Lim A, Morillon E, et al. Insertional oncogenesis in 4 patients after retrovirus-mediated gene therapy of SCID-X1. The Journal of clinical investigation 2008 Sep;118(9):3132-42.
5. Aiuti A, Slavin S, Aker M, Ficara F, Deola S, Mortellaro A, et al. Correction of ADA-SCID by stem cell gene therapy combined with nonmyeloablative conditioning. Science 2002 Jun 28;296(5577):2410-3.
6. Boztug K, Dewey RA, Klein C. Development of hematopoietic stem cell gene therapy for Wiskott-Aldrich syndrome. Current opinion in molecular therapeutics 2006 Oct;8(5):390-5.
7. Grez M, Reichenbach J, Schwable J, Seger R, Dinauer MC, Thrasher AJ. Gene therapy of chronic granulomatous disease: the engraftment dilemma. Molecular therapy : the journal of the American Society of Gene Therapy 2011 Jan;19(1):28-35.
8. Boztug K, Schmidt M, Schwarzer A, Banerjee PP, Diez IA, Dewey RA, et al. Stem-cell gene therapy for the Wiskott-Aldrich syndrome. The New England journal of medicine 2010 Nov 11;363(20):1918-27.
9. Braun CJ, Boztug K, Paruzynski A, Witzel M, Schwarzer A, Rothe M, et al. Gene therapy for wiskott-Aldrich syndrome–long-term efficacy and genotoxicity. Science translational medicine 2014 Mar 12;6(227):227ra33.
10. Larmonie NS, van der Spek A, Bogers AJ, van Dongen JJ, Langerak AW. Genetic and epigenetic determinants mediate proneness of oncogene breakpoint sites for involvement in TCR translocations. Genes and immunity 2014 Mar;15(2):72-81.
11. www.clinicaltrial.gov.
12. Aiuti A, Biasco L, Scaramuzza S, Ferrua F, Cicalese MP, Baricordi C, et al. Lentiviral hematopoietic stem cell gene therapy in patients with Wiskott-Aldrich syndrome. Science 2013 Aug 23;341(6148):1233151.
Adapiert nach Braun et al. Science of Translational Medicine 2014, Witzel et al Expert Opinion on Orphan Drugs 2013.
Mehr Informationen finden Sie hier:
Geschäftsstelle der Care for Rare Foundation für
Forschungsverbünde für Kinder mit seltenen Erkrankungen
seltene Erkrankungen
im Dr. von Haunerschen Kinderspital Administrationsbüro am Dr. von Haunerschen
Prof. Dr. Christoph Klein Kinderspital
Lindwurmstrasse 4 Lindwurmstr. 4
D-80337 München D-80337 München
Tel: +49/89-5160 5126 Tel: +49-89/5160 7700
E-Mail: info@research4rare.de E-Mail: info@care-for-rare.org
Web: www.research4rare.de Web: www.care-for-rare.org
Tipp: Aktuelle Weiterbildungsangebote zum Thema Medizin und Gesundheit finden Sie laufend online in der Bildungsdatenbank »medicine & health«.